5 Konsep Penting dalam Reaksi Redoks dan Elektrokimia – Postingan ini mengandung sumber jawaban yang dilontarkan oleh salah seorang mantan mahasiswi saya dulu. Sekalian saja saya jawab melalui postingan ini supaya bisa dibaca juga oleh siapa saja yang mungkin memerlukannya nanti. Reaksi Redoks (Reduksi-Oksidasi) memang pokok bahasan yang sedikit lebih ringan dibandingkan pokok bahasan lan dalam kimia. Bahkan lebih mudah memahaminya.
Berikut 5 konsep penting dalam reaksi redoks dan elektrokimia yang harus dipahami:
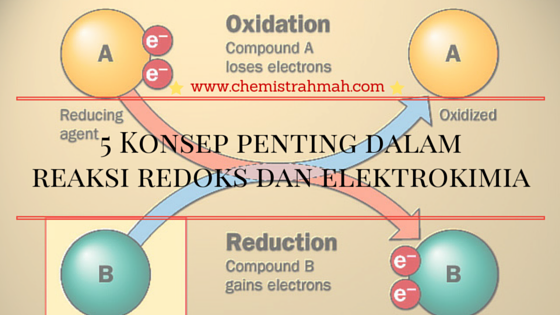
- Reaksi Redoks dan Elektrokimia; dalam bahasan ini harus diketahui bahwa persamaan reaksi redoks dapat disetarakan dengan metode ion-elektron. Dimana dalam reaksi redoks terjadi proses transfer elektron dari zat pereduksi ke zat pengoksidasi. Jika memakai komprtemen terpisah, maka reaksi redoks dapat digunakan sebagai penghasil sel galvanik (elektron mengalir pada bagian luar).
- Termodinamika Sel Galvanik; dalam bahasan ini harus dipahami bahwa voltase yang diukur dapat dipecah menjadi potensial elektroda dari anoda1 dan katoda2. Voltase kemudian bisa dihubungkan dengan perubahan energy bebas Gibbs dan konstanta keseimbangan dari proses redoks. Ada juga persamaan Nernst yang menghubungkan voltase sel galvanik ini dengan voltase sel pada keadaan standar atau spesi-spesi reaksi.
Dalam pembahasan ini juga bisa diketahui daftar nilai-nilai potensial reduksi standar, kespontanan reaksi redoks hingga efek konsentrasi pada Emf sel.
- Baterai; sebagaimana yang dipahami bahwa defines baterai adalah sel elektrokimia yang dapat mengambil arus listrik langsung pada voltase konstan. Di sini juga perlu diketahui pembahasan mengenai baterai sel kering (sel tanpa komponen cairan dan biasanya terdapat pada lampu senter dan radio transistor), baterai merkuri (digunakan dalam bidang pengobatan dan industri elektronik), baterai bertimbal (dikenal dengan Aki), sel bahan bakar (jenis sel elektrokimia khusus yang menghasilkan listrik dari proses oksidasi hidrokarbon atau hydrogen) dan juga baterai Litium dalam keadaan padat.
- Korosi; kalau di masyarakat dikenal dengan “karat”. Definisi lengkapnya adalah reaksi redoks spontan yang mengakibatkan terbentuknya karat dari besi, patina3 dari tembaga, perak sulfida dari perak. Adanya korosi bisa mengganggu dan mengakibatkan kerusakan pada bangunan, konstruksi, mobil, gedung dan kapal. Untuk itu diperlukan upaya untuk mencegah dan mengurangi dampak yang ditimbulkan oleh korosi.
- Elektrolisis; definisi elektrolisis adalah proses menjadikan reaksi redoks non-spontan bisa terjadi dengan bantuan energi listrik. Formula yang digunakan untuk menghitung besarnya arus yang dibutuhkan dengan produk yang dihasilkan adalah dengan rumus Faraday. Elektrolisis ini paling sering digunakan oleh industri-industri penting.
Jadi, pembahasan reaksi redoks atau reduksi oksidasi ringan dipelajari. Cukup menguasai 5 konsep penting dalam reaksi redoks dan elektrokimia di atas. Selain konsep di atas, harus latihan juga dalam menyetarakan reaksi redoks. Soal nilai dari potensial standar reduksi tidak perlu dihafalkan sebab jika sudah terbiasa maka angka-angka tersebut akan familiar. Nah, supaya ada interaktif, silakan menjawab soal berikut di kolom komentar. Tak perlu menyertakan reaksi.
Soal:
Apa yang akan terjadi jika molekul bromine ditambahkan pada larutan yang mengandung NaI pada suhu 25 derajat Celsius? Siapa yang bertindak selaku pengoksidasi dan pereduksi? *anggap semua spesi berada dalam keadaan standar.
Kalau ada yang sudah tahu jawabannya, jangan malu-malu jawab di kolom komentar. Benar atau salah, nanti dikoreksi bersama.
Catatan:
- Anoda: tempat reaksi oksidasi berlangsung
- Katoda: tempat reaksi reduksi berlangsung
- Patina: tembaga karbonat





One Response
aku blaaaas udah lupa pelajaran kimia mba…padahal dulu Fis 1 hehehehe